
LABOFUN.BE Specifieke warmtecapaciteit van een stof
Vanderwaalsbindingen ontstaan door vanderwaalskrachten. Er zijn drie soorten vanderwaalskrachten. Dipool-dipool interactie. In een molecuul is de lading niet altijd gelijk verdeeld, daardoor ontstaat er een positieve en een negatieve kant. Een atoom met een negatieve lading en een atoom met een positieve lading van een ander molecuul trekken.

Inleiding
Hoe kan je zien of een stof polair of apolair is? Het polair zijn van een molecule heeft te maken met de ladingsverdeling in de molecule. Wanneer deze symmetrisch is dan noemen we die molecule polair, is deze niet symmetrisch dan is ze apolair. Een halogeenalkaan heeft als achtervoegsel gewoon -aan. Als voorvoegsel gebruik je het betreffende.

Aristotle a book on Science
In de chemie vind je zowel polaire als apolaire stoffen terug. Er bestaan belangrijke verschillen tussen deze stoffen. Polaire stoffen hebben een + en - pool. Apolaire stoffen hebben geen lading. Ontdek de andere belangrijke verschillen in deze video!
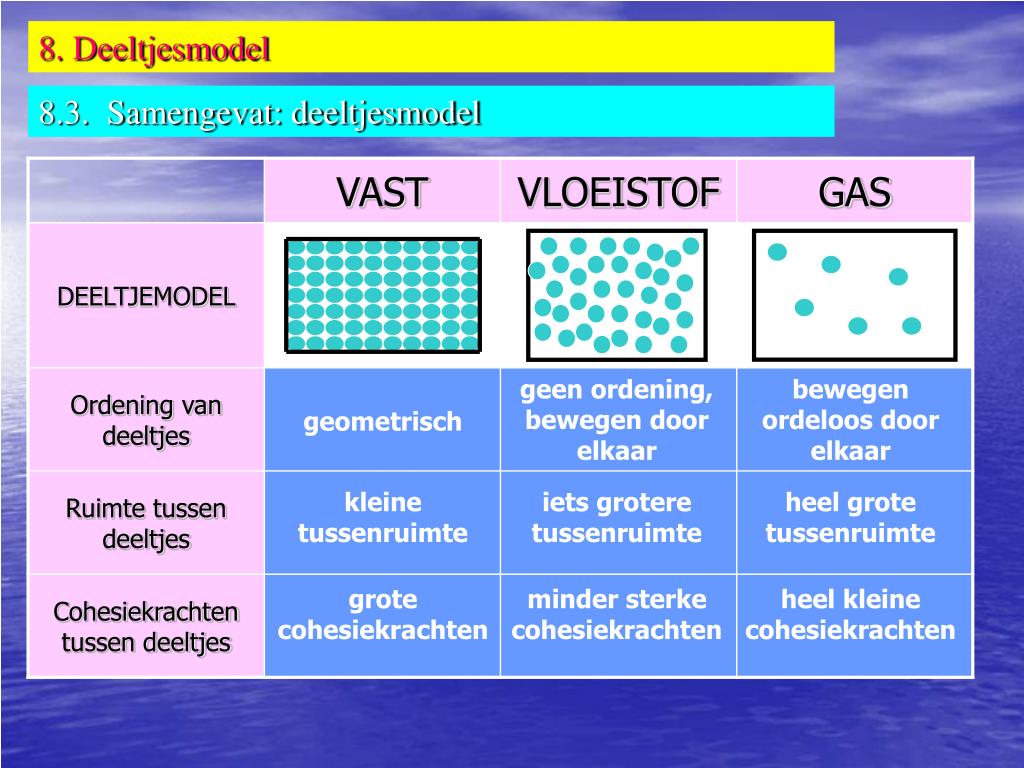
PPT Thema 4 Verfijning van het materiemodel atomen en moleculen PowerPoint Presentation ID
Een apolaire verbinding is het tegenovergestelde van een polaire verbinding. De mate waarin verbindingen polair zijn, wordt uitgedrukt in het dipoolmoment. Verbindingen met een polair en een apolair deel zijn amfifiel. Een voorbeeld van een apolaire verbinding is methaan (CH 4). Methaan is een apolaire verbinding omdat de (relatief positieve.

Invloed van apolaire staart op oplosbaarheid van alkanolen in water YouTube
Moleculen die geen verschil in lading hebben noemen we apolaire moleculen. De lading in een polair molecuul geven we aan met de griekse letter delta 𝛿 en een + of - teken. Moleculen die een polair zijn hebben een dipoolmoment en ze kunnen een dipool-binding aangaan. Polariteit ontstaat doordat de kern van het ene atoom hard trekt aan de.

Chemie hoofdstuk 3 polaire en apolaire moleculen Chemie hoofdstuk 3 oplossing in water Polaire
Een dipool-dipool interactie is relatief een vrij sterke binding. Het is een sterkere binding dan een vanderwaalsbinding. Alleen wanneer moleculen dipolen zijn, kan er zo'n interactie/binging optreden. Omdat zo'n binding relatief sterk is hebben stoffen die uit dipolen bestaan relatief hogere smelt- en kookpunten.

De polaire atoombinding en dipolen (kort) YouTube
Begrippen polair en apolair. Verschuiving van bindingselektronen. Polaire of apolaire binding. Symmetrische of asymmetrische moleculen Polair of apolair molecule. Quiz. Een UCLL project. Partners. Delen. Share. Email. Facebook; Ontworpen door Elegant Themes | Ondersteund door WordPress.
Elektriciteit Opbouw van een stof
We bevelen het gebruik aan van een moderne webbrowser zoals Chrome, Firefox, Safari of Edge. Wanneer is een molecule polair? Verander de elektro-negativiteit van atomen in een molecule om te zien hoe het de polariteit beïnvloedt. Bekijk hoe de molecule zich gedraagt in een elektrisch veld. Verander de bindingshoek om te bekijken hoe de vorm de.
Huishoudelijke apparaten Silicagel polair of apolair
Niet-polaire moleculen vormen zich ook wanneer atomen die een polaire binding delen , zodanig worden gerangschikt dat de elektrische ladingen elkaar opheffen. Voorbeelden van niet-polaire moleculen zijn onder meer: Elk van de edelgassen: He, Ne, Ar, Kr, Xe (Dit zijn atomen, geen technisch moleculen.) Elk van de homonucleaire diatomische.

LABOFUN.BE Specifieke warmtecapaciteit van een stof
Een polaire verbinding is een molecuul dat bestaat uit een chemische binding met een zodanige verdeling van de elektronen, dat het centrum van de negatieve ladingen niet samenvalt met dat van de positieve ladingen. Een polaire verbinding is het tegenovergestelde van een apolaire verbinding. Moleculen met zowel een polair als een apolair deel.
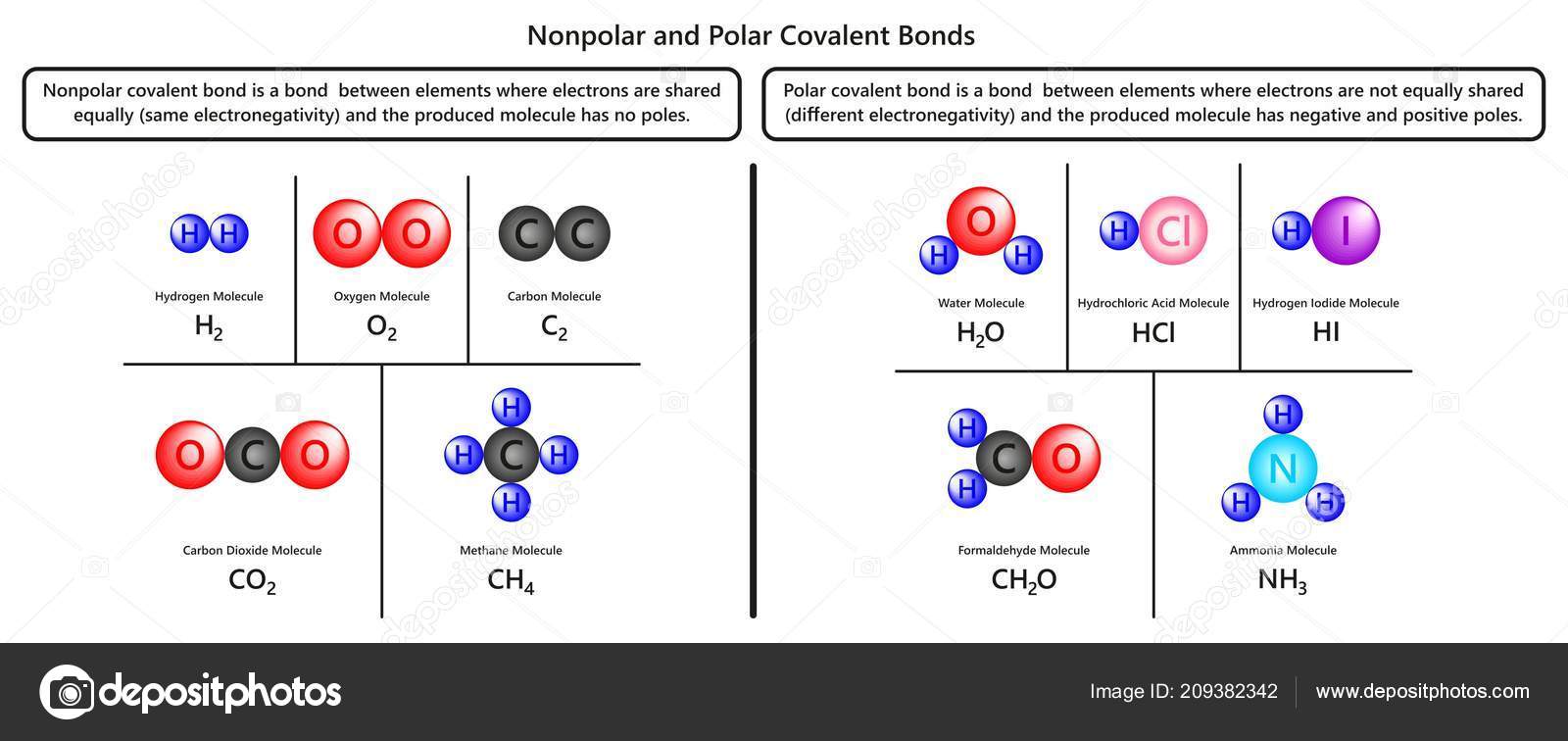
Ch4 Polar Or Nonpolar Covalent Bond Covalent bond Simple English Wikipedia, the free
Alleen: CO2 is symmetrisch en apolair terwijl lachgas niet symmetrisch is en een (klein) dipoolmoment heeft. Als je de kookpunten, smeltpunten en oplosbaarheden in water met elkaar vergelijkt kun je vaststellen wanneer het symmetrieverschil een rol speelt en wanneer niet. En let ook eens op het enorme verschil tussen vloeibaar Argon en.

LABOFUN.BE Specifieke warmtecapaciteit van een stof
In deze kennisclip legt Mimi van de Sistersinscience_NL je uit wanneer moleculen polair of apolair zijn, wat elektronegativiteit van een molecuul is, wat dipool-dipoolbindingen en wat waterstofbruggen zijn. Geen zin om een filmpje te bekijken? Hieronder lees je de tekst: Hallo allemaal, ik ben Mimi van de Sisters in Science en vandaag ga ik jullie […]

Verschil tussen polair en apolair moleculen met 2 atomen p 1013 YouTube
Polaire of apolaire stof. Dalton stelde als eerste vast dat atomen de kleinste deeltjes waren, waaruit een stof kon opgebouwd zijn. Thomson, Rutherford en Chadwick bewezen echter het tegendeel door het uitvoeren van talloze experimenten. Zo ontdekte Thomson dat er negatief geladen deeltjes voorkwamen in het atoom.

Bouw van de stof YouTube
Dat gebeurt wanneer een stof zich in een polair oplosmiddel bevindt, zij in een apolair oplosmiddel een lagere energietoestand zou hebben. In een mengsel van beide oplosmiddelen zal diffusie optreden van het polaire oplosmiddel naar het apolaire oplosmiddel.
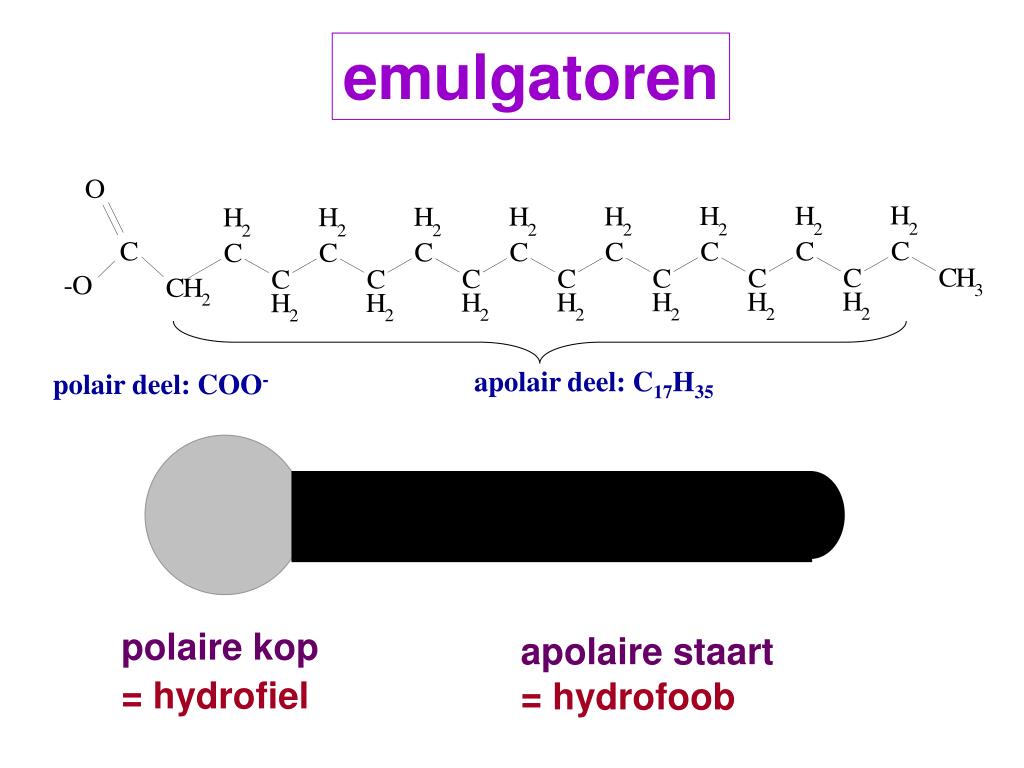
PPT Context 1 Materie, energie en leven PowerPoint Presentation, free download ID574150
Apolair of polair Een stof is polair wanneer deze een ladingsverschil heeft, het molecuul heeft een plus en een minkant en is dus een dipool-molecuul. Voorbeelden: fluormethaan, water en methanol. Een stof is apolair als de stof geen ladingsverschil heeft (de atoombindingen kunnen wel polair zijn maar de ladingen, vallen opgeteld weg)

MlavdBCEC1 Zure stoffen kennen we allemaal; bv azijn of ontkalker Wanneer is een stof zuur of
Transportprocessen. Alles in beweging. Transportprocessen. f. Concentratie of drukverschil. Een vloeistoffen of gassen verspreidt zich gelijkmatig over de beschikbare ruimte, Dat heet diffusie. Als water door een drukverschil diffundeert door een semipermeabel ofwel half doorlaatbaar membraan, dan heet dit osmose.
- What Is Kitchen Sink Realism
- Wat Is De Beste Vliegmaatschappij
- Hunger Games 3 Movie Cast
- Chinese Restaurant Den Haag Centrum
- Ing Groep Nv Annual Report
- Muddy Waters Hoochie Coochie Man
- Kosten Ticket Top 2000 Cafe
- Windsor Castle Windsor Verenigd Koninkrijk
- Arm Leg Leg Arm Head Meaning
- Muppet With A Long Curved Nose